细胞在运动、迁移、收缩、舒张和拉伸的过程中都会产生细胞牵引力(cell traction force, CTF)。这些力极其微小,但是它们却有着深刻的生物学影响,与生化信号一起协同有序地调控生命过程,在细胞增殖、分化、凋亡、肿瘤发生转移、伤口愈合以及胚胎发育中发挥关键作用。因此,了解细胞牵引力是如何影响细胞功能,不同状态下的细胞会产生多大的细胞牵引力,都对细胞生物学的研究十分重要。
近日,中科院北京纳米能源与系统研究所、北京航空航天大学生物医学工程高精尖创新中心、中国科学院大学和广西大学的研究团队共同研制出可实现心肌细胞的实时动态力成像的压电光电子学纳米“天线”阵列(Piezo-phototronic Light Nano-Antenna, PLNA),相关研究成果发表在最新一期(2021年5月26日)国际学术期刊Science Advances上。郑强博士、彭铭曾博士和刘卓博士为共同第一作者,李舟研究员,翟俊宜研究员和王中林院士为共同通讯作者。
该研究团队一直聚焦细胞牵引力的精确测量方法和器件研究。早在2009年,李舟和王中林就提出基于硅纳米线阵列测量细胞牵引力的方法,研究了正常细胞、良性和恶性肿瘤细胞的最大细胞牵引力的差异(Nano Letter, 2009, 9, 10:3575-3580)(图1)。通过利用扫描电子显微镜(SEM)获取硅纳米线阵列上由细胞引起的弯曲情况,结合纳米线的物理性能参数和位移数据进行统计分析,能够准确获得施加在纳米线上的细胞牵引力的大小。该工作是无机纳米线阵列在细胞牵引力研究中的新尝试,结合正常细胞和肿瘤细胞的细胞牵引力分析,对研究疾病的发生和发展过程提供了新的研究方法和技术手段。

图1 硅纳米线阵列量化细胞牵引力
2018年,基于细胞外基质(Extracellular matrix, ECM)对细胞牵引力的重要的影响,该研究团队通过优化硅纳米线阵列的参数与性能,探究细胞外基质对细胞牵引力的调控机理,并以MC-3T3成骨细胞为载体,系统研究了在亚微米空间分辨下细胞外基质调控成骨细胞牵引力的动态时序过程(Nano Energy, 2018, 50: 504-512)(图2)。该研究为理解细胞牵引力的动态时序变化过程以及ECM修饰的组织工程支架的构建提供了重要理论支撑。
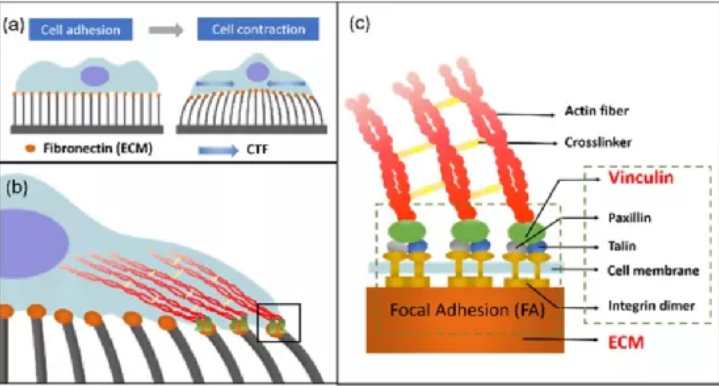
图2 细胞外基质对细胞牵引力的调控机理探究
在上述两个研究工作中,硅纳米线阵列在量化细胞牵引力及其调控机理方面取得了较好的进展,但是由于硅材料不透光,只能将细胞固定脱水后观察,这样就难以通过光学显微镜实时高分辨的观察细胞的动态变化过程。因此,实时、动态、快速、高分辨的活细胞牵引力测量成为下一步的研究目标。那么如何逐步实现这一目标呢?从2010年起,李舟和王中林就萌生了直接观察细胞爬行力的分布图的想法。
压电光电子学效应的提出为这项研究的推进提供了新思路和新方法。这一效应是由2010年王中林院士提出,其利用在压电半导体材料中施加应变所产生的压电电势来控制载流子在金属-半导体接触或者PN结处的产生、传输、分离或者复合,从而调控光电器件的光学性能。
2015年,该研究团队基于压电光电子学效应,首先构建了InGaN/GaN多量子阱的纳米线阵列(直径0.8 μm,高度1.2 μm,间距4 μm,分辨率为6350 dpi)。这种材料的使用首先解决了传统硅基材料不透光的问题,并且InGaN/GaN多量子阱的纳米线阵列在405 nm波长的激光激发下能够发光,发射波长为460nm。在压力/应变下产生的压电电荷成功调制了InGaN/GaN多量子阱的光致发光(Photoluminescence, PL)强度(图3)(ACS nano, 2015, 9, 3: 3143-3150)。
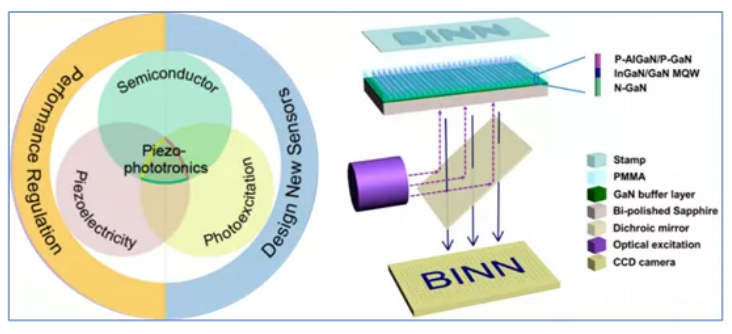
图3 压电光电子学理论导图以及压力/应变诱导产生压电电荷成功调制InGaN/GaN多量子阱的光致发光(Photoluminescence, PL)强度装置示意图
从硅纳米线到压电光电子学InGaN/GaN多量子阱纳米线,在材料本身获得改进的基础上,面向细胞牵引力的测量,其性能的提升至关重要。在本研究中,研究团队根据细胞牵引力的大小,结合材料的杨氏模量等数据,优化并改良工艺参数,以透光的蓝宝石为衬底,进一步减小InGaN/GaN多量子阱的纳米线的直径,提高长径比,优化纳米线阵列的单位密度,使之更加适配细胞牵引力的作用。最终制备的InGaN/GaN多量子阱的纳米线直径、高度和阵列间距分别为150 nm,1500 nm和800 nm(图4),空间分辨率达到31750 dpi,相较之前的器件,分辨率和性能都有大幅提升。

图4 InGaN/GaN多量子阱的纳米线形貌
为了探究该纳米线阵列是否可以实时动态的实现力成像,研究人员使用可自主收缩的心肌细胞为细胞牵引力的研究对象,通过心肌细胞的收缩和舒张运动,将细胞牵引力施加到细胞下部的压电光电子学纳米“天线”阵列上,其产生的正负压电电荷调制量子阱光致发光强度。通过激光共聚焦显微镜(confocal microscopy)对自主收缩的心肌细胞及其下部发光的纳米“天线”阵列进行动态成像,时间分辨率约333 ms,并建立细胞牵引力与光致发光强度变化的实时对应关系(图5),对细胞牵引力的测量范围可达0.17 μN-10 μN,检测灵敏度为15 nN/nm,同时具有良好的光学稳定性(抗光漂白)和重复性。
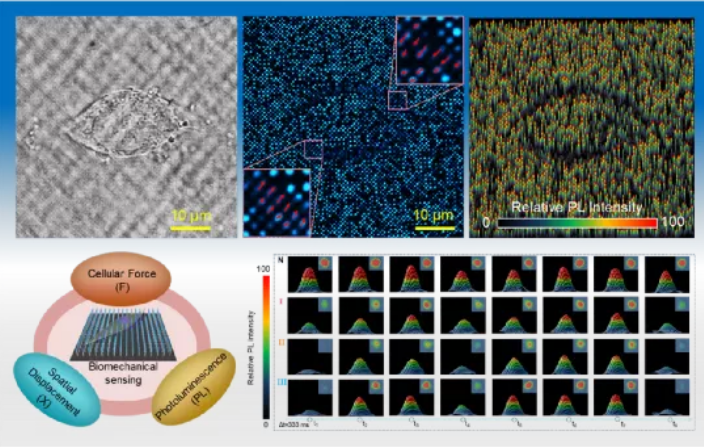
图5 通过InGaN/GaN多量子阱的纳米线构建细胞力与光致发光强度变化关系以及强度时阈变化图
该研究是首次基于压电光电子学效应提出一种超高空间分辨率实时测量细胞力分布的方法,是压电光电子学效应的又一独特的应用,并进一步证明了纳米线阵列在亚微米尺度上测量细胞牵引力的优异特性。该研究历时11年:从最初的固定脱水静态细胞分析到如今的实时动态活细胞分析;从硅基不透光材料到透明蓝宝石基底InGaN/GaN材料,简化了观测方法从扫描电子显微镜观察到激光共聚焦光学显微镜观察;从细胞周围纳米线的局部量化到细胞胞体覆盖的全域量化;从纳米线位移来测量细胞牵引力到压电光电子学InGaN/GaN多量子阱纳米线光强变化实时反馈细胞牵引力。该团队厚积薄发,“十年磨一剑”,逐步实现了实时、快速、动态、高分辨的细胞牵引力成像这一目标。它不但是生物工程探索中的一个重大进展,也是压电光电子学效应在医学中的一个崭新应用。与此同时,心肌细胞牵引力的动态精确测量,为心血管疾病相关的临床研究提供新的研究方法和平台,将深化对心肌细胞的生物力学特性以及心肌细胞之间、心肌细胞与胞外基质相互作用的理解,对疾病检测、药物筛选、组织工程和再生医学研究产生重要价值。